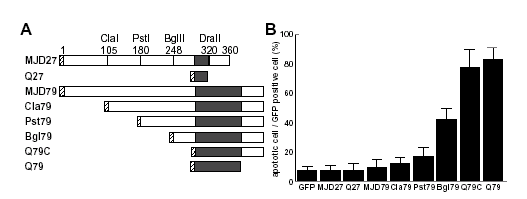
全長MJD蛋白質とその部分蛋白質での細胞死誘導活性の比較
(A) 実験に用いたさまざまな欠失変異蛋白質。塗りつぶされている部分がポリグルタミン。
(B) 欠失変異蛋白質をPC12細胞に一過性に発現させた際の細胞死誘導活性。N末端部分が 短くなり、伸長したポリグルタミン(この場合、Q79)そのものに近づくほど、細胞死誘 導活性が強現れる。死につつある細胞では、ポリグルタミンの凝集像が観察され、細胞死 誘導活性と凝集活性は密接にリンクしている。
(Kobayashi & Kakizuka, Cytogenet Genome Res., 2003)
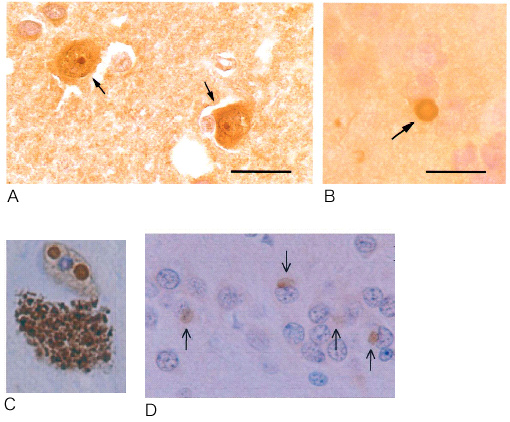
神経変性疾患に認められる細胞内の異常タンパク質の凝集体へのVCPの集積 ハンチントン病の核内封入体(A)、パーキンソン病のレビー小体(B)とマリネスコ 小体(C)さらには痴呆を伴った運動神経病の神経細胞内の凝集体(D)が抗VCP抗体で 陽性に染色された(矢印)。
(Hirabayashi et al., Cell Death Differ., 2001; Mizuno et al., Neurosci. Lett., 2003)
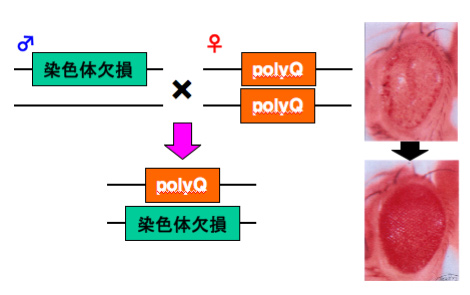
ter94遺伝子(VCPホモログ)の欠損は polyQの細胞死を抑制する
(Higashiyama et al., Cell Death Differ, 2002)
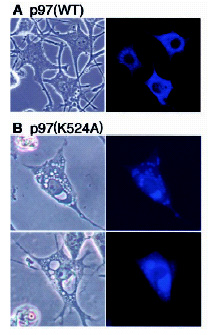
VCP(p97)のセカンドATP結合領域内に 変異を持つK524変異体PC12細胞に発現させると 細胞質の空胞形成が誘導される(左列)。 ERマーカータンパクを共発現させると、空胞と ERタンパクの局在が一致する(右列)。
(Kobayashi et al. J. Biol. Chem., 2002 )
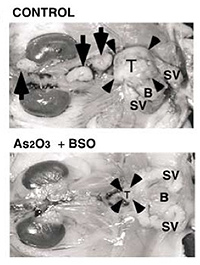
がん細胞をマウスの前立腺に接種し、control(上段)またはヒ素とBSOを投与して 7週間の写真 (下段)。
矢頭が成長した腫瘍を示し、矢印は転移した腫瘍である。
(Maeda et al., Cell Death Differ., 2003.)
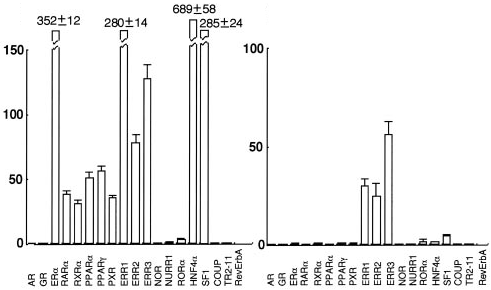
PGC-1αは、多くの核内受容体の転写を活性化させるpan核内受容体プロテイン・ リガンドとして機能すること(左)、一方、ERRL1/PGC-1βは、estrogen receptor-related receptor (ERR)に特異的な核内受容体プロテイン・リガンド(ERRL1)として機能することが判明した(右)。
(Kamei et al., Proc Natl Acad Sci, 2003.)
![]()